Правда, совсем недавно Робитайл и др. сообщили о результатах плацебо-контролируемого исследования фазы IIb, оценивающего влияние пищевой добавки MAG-EPA с длинноцепочечными ЖК омега-3 на пролиферацию рака простаты. Авторы показали, что ежедневная доза в три грамма MAG-EPA в течение 7 недель повышала в четыре раза уровень эйкозапентаеновой жирной кислоты в ткани простаты по сравнению с плацебо. Но, диетическая добавка не оказала влияния на первичный результат - пролиферацию РПЖ по экспрессии Ki-67. (Опубликовано 22 марта 2024 в журнале «Сommunications medicine»). Почему же нередко (а, практически всегда) мы получаем различные результаты, при идентичных или сравнимых условиях в исследованиях? Ответ понятен – мы не знаем и не можем учитывать все факторы, влияющие на итоговый результат. В этом аспекте всегда интересны исследования, которые выявляют механизмы, которые могут объяснить наличие эффекта или его отсутствие.
Большой интерес вызывает факт, что противораковые эффекты омега-3 ЖК зависят от микроокружения опухоли, а не от прямого воздействия на опухолевые клетки, а именно оказывают ингибирующее действие на функцию M2-подобных макрофагов. В модели мышей с раком простаты эффекты ингибирования роста рака посредством применения ω-3-диеты зависели от присутствия рецептора GPR120 в неопухолевых клетках организма, но не зависели от наличия GPR120 в клетках рака. Чтобы проверить эту гипотезу Пей Лян, Сюзанна М. Хеннинг и соавторы взяли мышей с трансплантированным раком предстательной железы (MycCap) и пересаживали им костный мозг от здоровых мышей или мышей с поврежденным геном рецептора GPR120 и потом кормили диетой с ω-3 или ω-6 ЖК. Авторы обнаружили, что диета ω-3 ингибировала рост аллотрансплантата MycCap только тогда, когда мышам-реципиентам вводили костный мозг от здоровых мышей-доноров. Дальнейшие рассуждения авторов привели к предположению, что пищевые ω-3 ЖК ингибируют прогрессирование рака простаты за счет воздействия на иммунные клетки, полученные из костного мозга, которые мигрируют в микроокружение опухоли и ими оказались инфильтрирующие опухоли М2-подобные макрофаги с рецептором GPR120.
Говоря кратко о микроокружении рака предстательной железы, то в нем присутствуют различные клеточные компоненты, в основном опухолеассоциированные макрофаги, ассоциированные с раком фибробласты, миелоидные супрессорные клетки которые играют решающую роль в онкогенезе, прогрессировании и метастазировании РПЖ. Более того, они в значительной степени опосредуют резистентность к традиционным методам лечения, включая антиандрогенную терапию, химиотерапию и иммунотерапию. Терапевтические вмешательства, направленные на эти клеточные компоненты, продемонстрировали многообещающие эффекты в доклинических моделях и нескольких клинических исследованиях. Xue-Feng Li, Cigdem Selliость et.al. обнаружили механизм устойчивости к энзалутамиду, зависящий от макрофагов. Эль-Кенави и его коллеги описали механизм, лежащий в основе резистентности опухолей простаты к гормональной терапии. Он включает накопление холестерина макрофагами в опухолях и его перенос в раковые клетки, где холестерин действует как предшественник андрогенов и приводит к активации андрогенных рецепторов, вызывая рост раковых клеток. Но проведенные попытки уменьшить количество макрофагов у пациентов с раком в клинических исследованиях не увенчались успехом, в основном из-за серьезных побочных эффектов.
Таким образом, сочетание диетической терапии, нацеленной на GPR120 в микроокружении, с терапией, нацеленной на опухоль, может быть полезным. Полученные доклинические результаты дают обоснование для клинических испытаний по оценке ω-3 ЖК в качестве потенциальной терапии рака простаты посредством ингибирования функциональных M2-подобных макрофагов GPR120.
Что в настоящее время дают полученные результаты пациентам в практическом применении? Ждать результаты исследований, или уже сейчас делать акцент в диете на ω-3 ЖК? С позиций доказательной медицины ответ однозначный – ждать результаты! Но, пока будут начаты и подведены результаты будущих исследований по данному вопросу, для многих пациентов время может уйти безвозвратно. Так что придется решать персонально, обсудив со своим лечащим онкологом.
Клинические испытания оправданы для оценки того, может ли диета на основе рыбьего жира задержать время развития резистентности к кастрации у мужчин, получающих андрогенную депривацию, тогда как необходимы дальнейшие исследования по оценке влияния рыбьего жира на прогрессирование рака простаты.
Таким образом, текущие исследования указывают на множество уникальных факторов, влияющих на ПК. Однако вопросы остаются, поскольку диета — это сложное и долгосрочное поведение. В конечном счете, остается ключевой вопрос без ответа: возможно ли разработать научно обоснованную диету для пациентов с ПК, которая достигает тройного эффекта, замедляет рост ПК, улучшает качество жизни и практична для внедрения с высоким уровнем одобрения?
Поскольку общественное мнение о диете постоянно меняется, возникают новые вопросы о диетических режимах и добавках, а также их связи с ПК. Играет ли воспалительный потенциал определенных диет какую-либо роль в риске ПК? Может ли ограничение углеводов повлиять на рост опухоли? Безопасны ли диеты, имитирующие голодание, которые эффективны при лечении диабета 2 типа и метаболического синдрома, и для контроля веса у пациентов с ПК?
Кроме того, поиск пищевой добавки с профилактическим действием на ПК пока не дал положительных результатов [ 2 ]. Хотя четкие доказательства рекомендуемого использования отсутствуют, поиск добавок для профилактики ПК продолжается с использованием жирных кислот омега-3.
За счет воздействия на иммунные клетки, полученные из костного мозга с функциональным GPR120, которые мигрируют в микроокружение M2 в макрофагах GFP+, инфильтрирующих опухоль CD206+, которые, как известно, связаны с прогрессированием рака простаты, снижалась только тогда, когда M2-подобные макрофаги. Таким образом, клетки костного мозга хозяина с функциональным GPR120 необходимы для противоракового действия пищевых ω-3 ЖК, а ключевой мишенью ω-3-диеты являются M2-подобные CD206+ макрофаги. А ключевой мишенью ω-3-диеты являются M2-подобные CD206+ макрофаги.
Только M2-подобные макрофаги были снижены в количестве в группах с диетой ω-3 по сравнению с ω-6. Аналогичным образом, экспрессия генов маркеров M2 в макрофагах GFP+, инфильтрирующих опухоль CD206+, которые, как известно, связаны с прогрессированием рака простаты, снижалась только тогда, когда M2-подобные макрофаги имели функциональный GPR120. Таким образом, клетки костного мозга хозяина с функциональным GPR120 необходимы для противоракового действия пищевых ω-3 ЖК, а ключевой мишенью ω-3-диеты являются M2-подобные макрофаги.
GPR120 представляет собой рецептор, участвующий в модуляции метаболизма, эндокринной и иммунной функций, и является рецептором для длинноцепочечных полиненасыщенных жирных кислот.

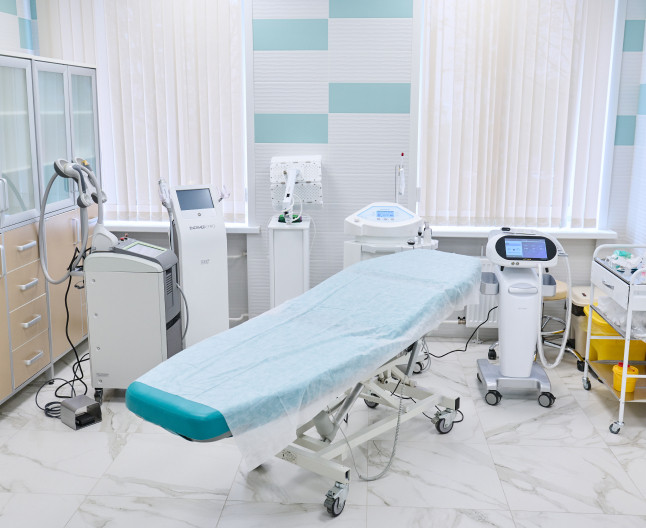
















Участие опухолеассоциированных макрофагов и зависимость от GPR120 в опухолевом микроокружении.
Хотя исследования, связывающие диету и рак, не новы, недавние исследования показывают, что диетические факторы и ожирение связаны как с риском возникновения, так и с исходами рака простаты, тем самым открывая дополнительные перспективы контроля заболевания.
В многочисленных доклинических моделях, в том числе на животных, пищевые ω-3 жирные кислоты (ЖК) из рыбьего жира задерживали развитие и прогрессирование андроген-чувствительного и кастрат-резистентного рака предстательной железы (РПЖ). Однако эпидемиологические исследования на людях сообщают о различных результатах влияния ЖК на риск развития данного рака. В проспективном исследовании у мужчин с РПЖ, которые проходили активное наблюдение более высокие уровни эйкозапентаеновой кислоты в ткани простаты коррелировали с меньшим вероятность развития агрессивной формы РПЖ при последующих биопсиях. Аналогичным образом, исследование перед простатэктомией сообщило о снижении пролиферации (индекс Ki-67) и снижении показателя генетического риска в опухолевой ткани после простатэктомии у мужчин соблюдающих диету с низким содержанием жиров и потребляющие добавки рыбьего жира по сравнению с так называемой западной диетой.